Tabela Periódica PDF – Completa para Imprimir — Atualizado 2025 com todos os 118 elementos
FERRAMENTAS PRONTAS
TABELA PERIÓDICA EM PDF COMPLETA PARA IMPRIMIR
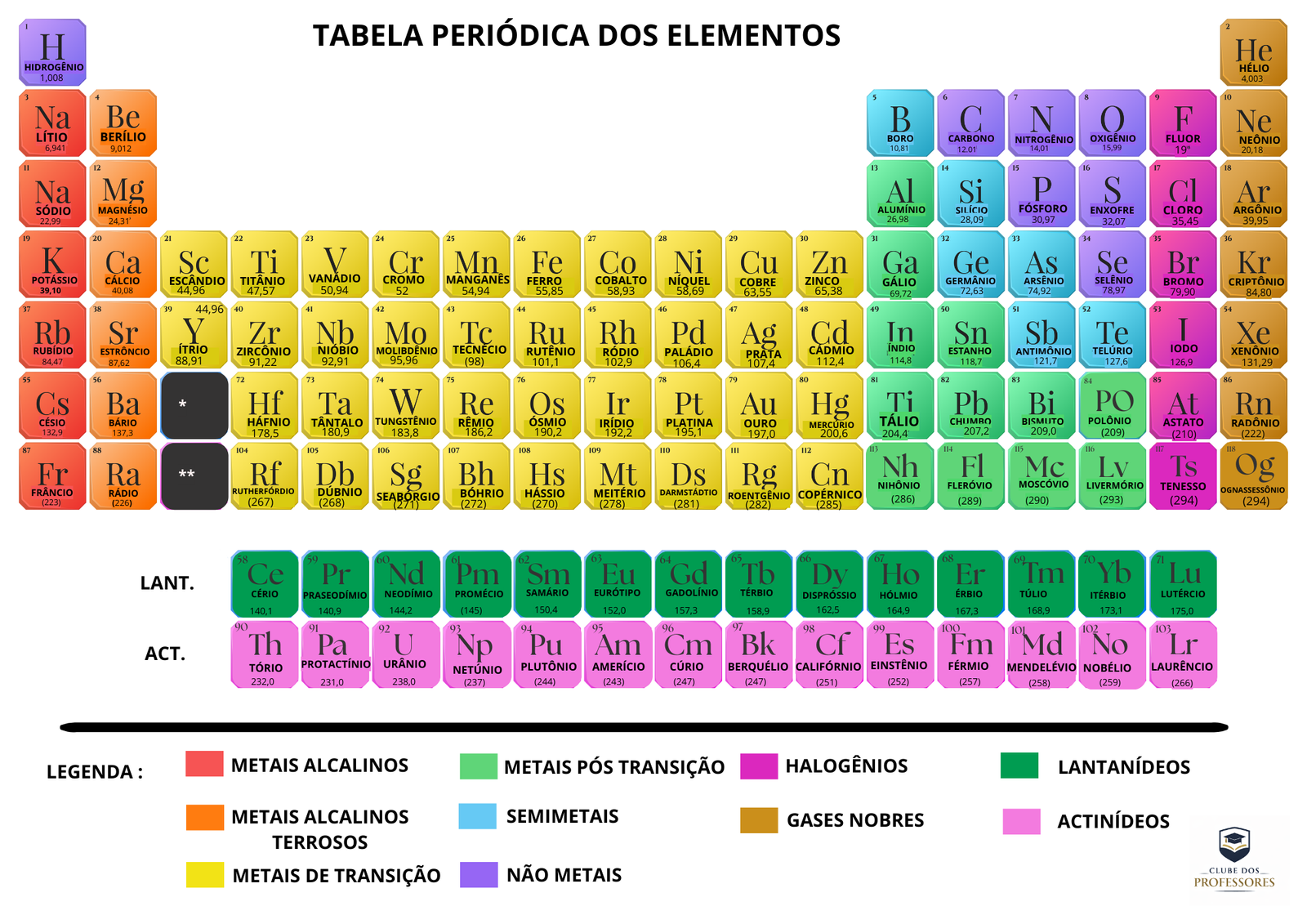
Tabela Periódica A4 – COLORIDA
DESCRIÇÃO : Para uso pessoal do professor, fácil visualização durante a aula.
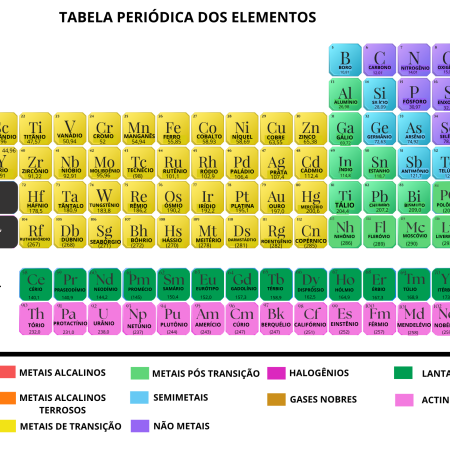
Tabela Periódica A4 – PRETO E BRANCO
DESCRIÇÃO : Para uso pessoal do professor, fácil visualização durante a aula, versão econômica, preto e branco.
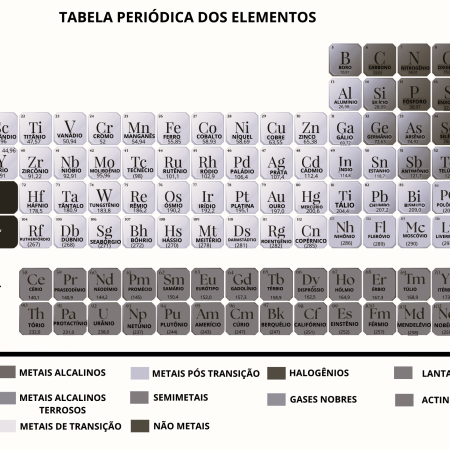
Tabela Periódica A3 – COLORIDA
DESCRIÇÃO : Para uso em explicações e demonstrações para a turma durante a aula, versão A3, mais visual.
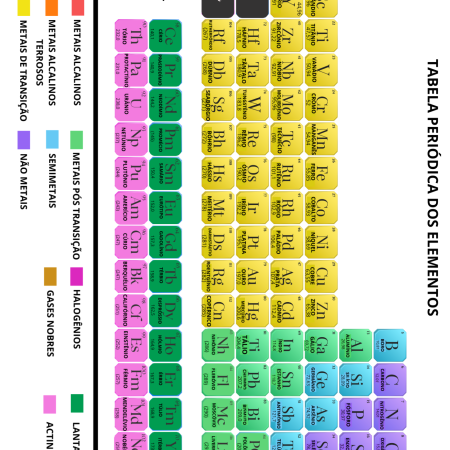
Tabela Periódica VERSÃO ALUNOS – COLORIDA
DESCRIÇÃO : Para impressão e distribuição para o aluno colar no caderno, dimensão A5.
Como ler a Tabela Periódica: o que significa cada informação do elemento
A Tabela Periódica parece complexa na primeira vez — mas ela segue uma lógica muito clara. Cada caixinha que representa um elemento traz exatamente quatro informações essenciais. Entender o que significa cada uma é o primeiro passo para ensinar esse conteúdo com segurança.
Veja o que está em cada elemento:
Informação | O que significa |
Número atômico (Z) | Quantidade de prótons no núcleo — define a identidade do elemento |
Símbolo químico | Abreviação internacional do elemento — igual em todo o mundo |
Nome do elemento | Nome completo em português |
Massa atômica | Média da massa dos isótopos do elemento, em unidades de massa atômica (u) |
O que são os Períodos da Tabela Periódica?
Os períodos são as linhas horizontais da tabela — são 7 no total. O número do período indica quantas camadas eletrônicas o átomo possui. Por exemplo, todos os elementos do período 2 têm dois níveis de energia ao redor do núcleo.
Isso significa que, ao longo de um mesmo período da esquerda para a direita, os elementos mudam de características químicas mas mantêm o mesmo número de camadas.
O que são os Grupos (ou Famílias) da Tabela Periódica?
Os grupos são as colunas verticais — são 18 no total. Elementos do mesmo grupo compartilham o mesmo número de elétrons na camada mais externa (camada de valência) e por isso têm comportamento químico semelhante.
Os grupos mais importantes para o Ensino Fundamental II:
Grupo 1 — Metais Alcalinos: muito reativos, reagem violentamente com água
Grupo 2 — Metais Alcalino-terrosos: menos reativos que o grupo 1
Grupo 17 — Halogênios: muito reativos, formam sais ao reagir com metais
Grupo 18 — Gases Nobres: praticamente não reagem com nada — camada de valência completa
Quer ensinar Tabela Periódica sem montar a aula do zero?
Acesse o plano de aula completo para o 9º ano — roteiro palavra por palavra, atividade prática e gabarito incluídos
As famílias da Tabela Periódica: o que são e como ensinar cada uma
A Tabela Periódica é dividida em famílias de elementos com características em comum. Ensinar pelas famílias é mais eficiente do que decorar elemento por elemento — o aluno entende a lógica e consegue prever o comportamento de elementos desconhecidos.
Metais Alcalinos — Grupo 1
Lítio, Sódio, Potássio, Rubídio, Césio e Frâncio. São os metais mais reativos da tabela. O Sódio (Na) e o Potássio (K) são ótimos exemplos do cotidiano — presentes no sal de cozinha e em alimentos. Reagem com água liberando hidrogênio e calor — um vídeo desse experimento funciona muito bem em sala para prender a atenção.
Metais Alcalino-terrosos — Grupo 2
Berílio, Magnésio, Cálcio, Estrôncio, Bário e Rádio. Menos reativos que os alcalinos. O Cálcio (Ca) é o exemplo mais familiar — presente nos ossos e no leite. O Magnésio (Mg) aparece nos antiácidos estomacais. São conexões fáceis de fazer com o cotidiano dos alunos.
Metais de Transição — Grupos 3 a 12
O maior bloco da tabela. Inclui elementos como Ferro (Fe), Cobre (Cu), Ouro (Au), Prata (Ag) e Zinco (Zn). São os metais que os alunos mais conhecem no dia a dia — moedas, fios elétricos, joias, ferramentas. Ótimo ponto de entrada para tornar o conteúdo concreto.
Semimetais (Metaloides)
Boro, Silício, Germânio, Arsênio, Antimônio, Telúrio e Polônio. Têm propriedades intermediárias entre metais e não metais. O Silício (Si) é o mais importante — base de todos os semicondutores e chips eletrônicos. Perfeito para conectar com tecnologia e despertar interesse nos alunos.
Não Metais
Hidrogênio, Carbono, Nitrogênio, Oxigênio, Fósforo, Enxofre e Selênio. Fundamentais para a vida. O Carbono (C) é o elemento base de toda a química orgânica. O Oxigênio (O) e o Nitrogênio (N) compõem a maior parte do ar que respiramos. São os elementos mais presentes nos organismos vivos.
Halogênios — Grupo 17
Flúor, Cloro, Bromo, Iodo e Astato. Muito reativos e tóxicos em estado puro — mas formam compostos essenciais para a vida. O Cloro (Cl) é usado no tratamento de água potável. O Flúor (F) está na pasta de dente. O Iodo (I) é fundamental para o funcionamento da tireoide.
Gases Nobres — Grupo 18
Hélio, Neônio, Argônio, Criptônio, Xenônio e Radônio. São chamados de nobres porque praticamente não reagem com outros elementos — têm a camada de valência completa com 8 elétrons (exceto o Hélio com 2). O Hélio enche balões. O Neônio é usado em letreiros luminosos. São ótimos exemplos visuais para a aula.
Lantanídeos e Actinídeos
As duas linhas separadas na parte inferior da tabela. Os lantanídeos (57 a 71) são usados em telas de celular, imãs e lasers. Os actinídeos (89 a 103) incluem elementos radioativos como Urânio (U) e Plutônio (Pu). Para o Fundamental II, basta apresentar que existem e explicar por que ficam separados — o tamanho da tabela ficaria impraticável se fossem inseridos no bloco principal.
O que são os períodos da Tabela Periódica e como usar isso em sala de aula
Existem 7 períodos na Tabela Periódica — cada linha horizontal representa um período. O número do período indica diretamente quantas camadas eletrônicas o átomo daquele elemento possui.
Período | Camadas eletrônicas | Exemplo de elemento |
1 | 1 camada (K) | Hidrogênio (H), Hélio (He) |
2 | 2 camadas (K, L) | Carbono (C), Oxigênio (O) |
3 | 3 camadas (K, L, M) | Sódio (Na), Alumínio (Al) |
4 | 4 camadas (K, L, M, N) | Ferro (Fe), Cobre (Cu) |
5 | 5 camadas | Prata (Ag), Iodo (I) |
6 | 6 camadas | Ouro (Au), Chumbo (Pb) |
7 | 7 camadas | Urânio (U), Plutônio (Pu) |
Como simplificar para alunos do 9º ano: o número do período é igual ao número de camadas do átomo. Basta olhar em qual linha o elemento está. Não é necessário decorar — a própria tabela já informa.
5 dicas práticas para ensinar Tabela Periódica sem perder os alunos
1. Comece pelos elementos que os alunos já conhecem
Antes de apresentar a tabela inteira, pergunte: que materiais vocês usam no dia a dia? Ferro na mochila, alumínio na lancheira, oxigênio no ar, cálcio no leite, cloro na piscina. Localize esses elementos na tabela juntos. O aluno percebe que a tabela não é abstrata — está ao redor dele.
2. Use a tabela colorida como ferramenta ativa, não como decoração
Distribua a tabela impressa colorida por famílias e proponha uma tarefa simples: circule todos os elementos que você já ouviu falar. Depois compara com a turma. Isso gera engajamento imediato e mostra ao aluno o quanto ele já sabe antes mesmo da aula começar.
3. Evite a decoreba — ensine a lógica
O maior erro no ensino da Tabela Periódica é pedir para os alunos memorizarem elementos. O foco deve ser ensinar a ler a tabela — entender o que o número atômico significa, por que elementos do mesmo grupo se comportam de forma parecida, o que o período indica. Um aluno que entende a lógica consegue responder qualquer questão com a tabela na frente.
4. Conecte com notícias e tecnologia
Lítio nas baterias de celular. Silício nos chips. Ouro nos conectores eletrônicos. Hélio nos exames de ressonância magnética. A Tabela Periódica está em cada aparelho que os alunos usam. Trazer essa conexão transforma um conteúdo que parece distante em algo relevante para o cotidiano deles.
5. Use a seção ‘Se der errado’ antes da aula
Os problemas mais comuns no ensino de Tabela Periódica: alunos confundindo período com grupo, confundindo massa atômica com número atômico, e achando que elementos do mesmo período têm propriedades parecidas (quando na verdade são os do mesmo grupo). Antecipar esses erros na sua preparação evita que eles apareçam durante a aula.
Quer uma aula de Tabela Periódica já estruturada, com experimento e gabarito?
Temos o plano de aula completo pronto para você aplicar amanhã.
Perguntas frequentes sobre a Tabela Periódica
Quantos elementos tem a Tabela Periódica?
A Tabela Periódica tem atualmente 118 elementos confirmados, organizados por número atômico crescente. O último elemento a ser oficialmente nomeado foi o Oganessônio (Og, elemento 118), confirmado pela IUPAC em 2016.
Como os elementos são organizados na Tabela Periódica?
Os elementos são organizados por número atômico crescente — da esquerda para a direita e de cima para baixo. Elementos com propriedades químicas semelhantes ficam na mesma coluna (grupo). Essa organização foi proposta por Dmitri Mendeleev em 1869 e aperfeiçoada ao longo dos anos.
Qual a diferença entre período e família (grupo)?
Período é a linha horizontal — indica o número de camadas eletrônicas do átomo. Família ou grupo é a coluna vertical — elementos do mesmo grupo têm o mesmo número de elétrons na camada mais externa e por isso têm comportamento químico semelhante.
O que é número atômico?
O número atômico (Z) é o número de prótons no núcleo do átomo. É o que define a identidade do elemento — dois átomos com o mesmo número de prótons são sempre o mesmo elemento químico, mesmo que tenham massas diferentes (isótopos).
O que é massa atômica?
A massa atômica é a média ponderada das massas de todos os isótopos naturais de um elemento, expressa em unidades de massa atômica (u). É o valor decimal que aparece abaixo do símbolo na tabela — como 12,01 para o Carbono ou 55,85 para o Ferro.
Por que lantanídeos e actinídeos ficam separados na parte de baixo?
Por uma questão de espaço e praticidade. Se fossem inseridos em suas posições corretas — entre os grupos 2 e 3 — a tabela ficaria muito larga para ser impressa ou visualizada. A separação é uma convenção gráfica adotada mundialmente, não uma diferença de organização conceitual.
Qual foi o último elemento descoberto?
O Oganessônio (Og), de número atômico 118, foi o último elemento a receber nome oficial pela IUPAC em 2016. É um elemento sintético extremamente instável — não existe na natureza e só foi produzido em laboratório em quantidades muito pequenas.
Receba materiais gratuitos de Ciências no seu email
Cadastre-se e receba imediatamente um plano de aula completo de Tabela Periódica no seu email — com roteiro, atividade prática e gabarito. Sem spam. Cancele quando quiser.
COMENTÁRIOS :
Show, ajudou muito!
Fátima
São Miguel Paulista
Parabéns pela organização pessoal
Marcelo Paiva
Paulínia
bom!
Maria de Fátima
Monte Azul